수소이온은 어떻게 생기는 것일까? 물 때문이다. 물은 H2O다. 물에는 H2O만 있는 게 아니다. H2O가 분리되어 수소이온(H+)과 수산이온(OH-)이 생겨 H2O, H+, OH- 이렇게 ‘한 지붕 세 가족’이 된다. 중성에서는 수소이온과 수산이온의 수가 같아서 pH는 7.0이지만 수도꼭지에서 나오는 물을 측정해보면 이보다 낮은 6.0정도에 지나지 않는다. 왜냐하면 공기 속에 있는 탄산가스(CO2)가 물에 잘 녹아 들어가기 때문이다. 녹아 들어간 탄산가스는 물과 작용해서 수소이온을 만들어낸다.
흙 속에 있는 성분 중에 누가 가장 힘이 세고, 두 번째, 세 번째는 어떤 성분일까? 힘의 세기는 이렇다.
수소≥칼슘>마그네슘>칼륨≥암모늄>소디움>리튬
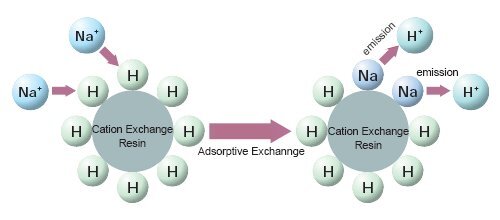
제일 강한 것은 수소이고 제일 약한 것은 리튬이다. 제일 강하면서 해가 되는 수소를 물리칠 만한 것은 칼슘밖에 없다. 칼슘이 많이 들어 있는 비료는 석회다. 그래서 우리는 석회에 주목할 필요가 있다. 흙에 준 비료는 흙알갱이에 붙는다. 마치 자석에 쇳가루가 붙는 것처럼 양분이 흙알갱이에 붙는다. 마구 아무렇게나 붙는 것이 아니라 자리 수가 정해져 있어 일정한 수만 붙을 수 있다. 이런 자리를 수소이온이 점령한다.
식물이 양분을 흡수할 때 어떤 꼴로 흡수할까? 우리가 밥을 먹으면 제일 먼저 침이 나와 녹말을 녹인다. 위장으로 들어가면 각종 효소가 나오고 위장이 운동해서 음식물과 효소가 잘 섞이게 한다. 시간이 지나면 음식은 장에서 흡수될 수 있는 극히 작은 화학 성분으로 변한다.
흙 속에서도 이와 매우 흡사한 일들이 일어나고 있다. 퇴비를 주면 흙 속의 미생물이 공격한다. 퇴비가 분해되면서 각종 화학 성분이 떨어져 나온다. 화학 성분은 다시 이온으로 되어야 비로소 뿌리가 빨아먹을 수 있다.
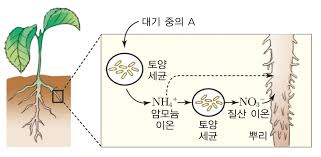
요소 알갱이는 (NH2)2CO라는 화학물질의 덩어리다. 흙 속에서 요소는 2개의 NH2+와 1개의 CO2-로 분해된다. NH2+는 미생물의 작용을 받아서 NH4+나 NO3-로 변한 후 뿌리에 들어간다. 칼리질 성분은 염화칼리로 준다. 염화칼리는 KCl의 덩어리다. KCl은 물에 녹아 K+와 Cl-로 분리된다. 이런 상태에서야 뿌리는 칼륨(K)과 염소(Cl)를 빨아먹을 수 있다. 제 아무리 잘난 뿌리라도 KCl을 그대로 빨아먹지는 못한다.
질소비료가 뿌리로 들어갔다고 말하면 우리는 머릿속에 ‘NO3-'나 ’NH4+'가 들어갔다고 연상하고, 칼륨이 들어갔다고 말하면 ‘K+'가 들어갔다고 연상할 수 있어야 한다. 수경재배나 양액재배를 하면서 이런 개념을 모르면 어려움이 많다.
| 식물에 필요한 양분과 흡수되는 꼴 | ||||
| 원소 | 흡수형태 | 원자번호 | 원자량 | 건물증 함량(%) |
| 수소 | H2O | 1 | 1.01 | 6 |
| 탄소 | CO2 | 6 | 12.01 | 45 |
| 산소 | O2, H2O | 8 | 16.00 | 45 |
| 질소 | NO3-, NH4+ | 7 | 14.01 | 1.5 |
| 칼륨 | K+ | 19 | 39.10 | 1.0 |
| 칼슘 | Ca2+ | 20 | 40.08 | 0.5 |
| 마그네슘 | Mg2+ | 12 | 24.31 | 0.2 |
| 인 | H2PO42-HPO42- | 15 | 30.97 | 0.2 |
| 황 | SO42- | 16 | 32.06 | 0.1 |
| 염소 | Cl- | 17 | 35.45 | 0.01 |
| 붕소 | BO33-, B4O72- | 5 | 10.8 | 0.00215 |
| 철 | Fe3+, Fe2+ | 26 | 55.85 | 0.01 |
| 망간 | Mn2+ | 25 | 54.94 | 0.005 |
| 아연 | Zn2+ | 30 | 65.38 | 0.002 |
| 구리 | Cu2+, Cu+ | 29 | 63.55 | 0.0006 |
| 몰리브덴 | MoO2- | 42 | 95.94 | 0.00001 |